- 国际物流聚合平台简介
- 货兜资讯
NEWS
| 口罩等防疫物品出口,需要哪些资质?走哪条路线比较好? | ||||||||||||||||||
| 2020-03-12 11:37:47.0 | ||||||||||||||||||
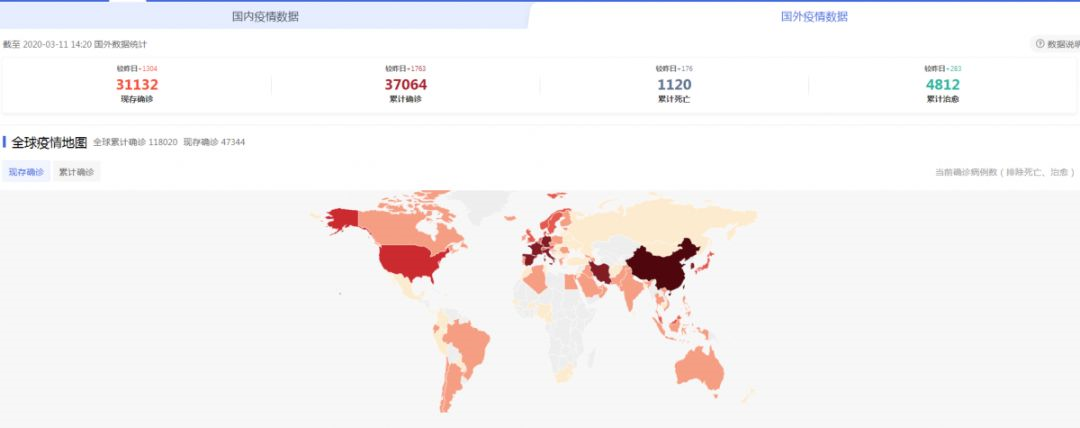
中国的疫情,在政府的运筹帷幄中和人民的通力合作下,得到了较好的控制,生活和工作渐渐开始走上正轨。 然而,国外的疫情却越来越严重…… 截止至2020年3月11日,国外已累计确诊人数37064例!其中,意大利、韩国、伊朗、美国等地情况都不容乐观。
最近货兜遇到了许多要出口口罩等防疫物资的客户,整理出以下几个常见问题和答案,希望对各位朋友有所帮助。 根据商务部消息,我国目前未对口罩设置任何贸易管理措施! 也就是说,只要你操作正当,走流程,有资质,海关是不会卡你的。但是根据客户的经历,建议最好少量 (50kg以下)出口,不然容易被退回。 普通口罩等非医疗器械管理的疫情物资,没有监管条件,有进出口权的企业,就可以直接出口。 涉证的口罩等疫情物资,需要产品三证:A.营业执照(经营范围包含有医疗器械相关)、B.产品备案证或者 注册证、C. 厂家检测报告,然后有进出口经营权的企业,再行出口。 另外,如果是企业想赠送或者代替海外关联公司采购,需要提供情况说明。 一定要符合其他国家的标准,不然你的物资是进不去的。 出口日本要在PMD Act的要求下,TOROKU注册系统要求国外的制造商必须向PMDA注册制造商信息。 出口韩国需要标注原产地,并且需要有KF认证。 出口美国的口罩,必须有FDA认证。 出口欧洲的口罩必须有CE认证。 如果你的口罩是具备三证的工厂产出的,可以通过外贸代理进行出口销售,如果没有三证,那就无法出口了。 普通口罩和医用口罩是指用途。而药监局管理是按照产品品和标准来管理的。二类和三类医疗器械的口罩, 需要备案证或注册证才能出口。涉证口罩所需的证件,见第2个问题。 贸易公司没有医疗器械的资质可以出口口罩吗? 厂家可以提供三证,退税有问题吗? 可以的,厂家提供三证是完全可以出口的。当然外贸公司的营业范围最好包括劳防用品等内容,这样, 出口退税会更有保障。 个人行邮目前也是不禁止出口的。一般快递美国,可以考虑FedEx、UPS、DHL、SF等快递公司。 不过有人反映,DHL会要求寄件人提供美国的FDA认证,也有的DHL干脆拒收,也有的被FedEx拒收过。 所以各位朋友要寄的时候也可以先尝试邮局邮寄,或者在邮寄前,先电话咨询各个快递公司。 熔喷布并不属于医疗器械,因此不需要医疗器械证明。具体可前往国家食药监局官网查询。 官网网址:http://samr.cfda.gov.cn/WS01/CL1026/ 进口伊朗还是比较复杂的,需要在伊朗申请COI认证,中文为符合性核查,是伊朗进口强制发件要求的相关检查。 目前伊朗N95口罩和普通三层口罩、呼吸器、手术服、核酸检测试剂盒、个人防护用品、防护面罩和 防护服等物资告急。 为鼓励进口,2月26日伊朗《经济在线》报道,伊朗市场口罩的进口关税从55%降到了5%。 物资商品编码参考 ↓
韩国 必要资料(资质):提单、箱单、发票。 韩国进口营业执照,韩国收货人需要到韩国药监局提前备案进口资质,官网www.kpta.or.kr。 企业自用又是受赠的情况,可以自行进口,不需要有相关资质。 口罩要求: 口罩还需要有详细的原产地标识,如果是中国制造务必有标签:Made In China、生产厂家信息、保质期, 还要准备成分含量说明,制造工艺流程,不止如此,等到货物到韩国后还需要将检测化验样品, 化验合格后方可进入韩国市场销售流通。 韩国医用防护 (标准依据MFDSNotice NO.2015-69): 1.过滤效率80% KF80防沙尘口罩 2.过滤效率94% KF94防疫口罩 3.过滤效率99% KF99卫生保健口罩 日本 必要资料(资质):提单、箱单、发票。 出口日本的PMDA注册医疗器械公司希望把产品投放到日本市场,必须要满足日本PMD Act的要求, TOROKU注册系统要求国外的制造商必须向PMDA注册制造商信息。 口罩要求: 包装上印有ウィルスカット99%的字样都是超过国内过滤效率95%(N95口罩)标准的医用口罩。 PFE:0.1um微粒子颗粒过滤效率 BFE:细菌过滤率 VFE:病毒过滤率 ウィルスカット:病毒拦截 医用防护口罩:符合中国GB19083-2010强制性标准,过滤效率≥95%(使用非油性颗粒物测试)。 N95口罩:美国NIOSH认证,非油性颗粒物过滤效率≥95%。 KN95口罩:符合中国GB2626强制性标准,非油性颗粒物过滤效率≥95%。 美国 必要资料(资质):提单、箱单、发票。 口罩要求: 美国进口的口罩,若需要销售,必须要拿到FDA认证才可以在美国本土市场进行销售活动。 对于自用和赠送的口罩,大家在出口的时候最好先问一下美国接收方,是否也需要FDA认证, 或者采购原本就通过FDA认证的口罩进行出口。
根据HHS(美国卫生及公共服务部)法规,NIOSH(美国国家职业安全卫生研究所)将其认证的防颗粒物 口罩分为9类。具体的认证则由NIOSH下属的NPPTL 实验室操作。 在美国,按过滤网材质的最低过滤效率,可将口罩分为三种等级——N 、R 、P: ▶N类口罩只能过滤非油性颗粒物,比如:粉尘、酸雾、漆雾、微生物等。空气污染中的悬浮微粒,也多是非油性的。 ▶R类口罩只适合过滤油性颗粒物及非油性颗粒物,但用于油性颗粒物时限制使用时间不得超过8小时。 ▶P类口罩则既可过滤非油性颗粒物,又可过滤油性颗粒物。油性颗粒物比如:油烟、油雾等。 根据过滤效率的不同,又有90、95、100的差别,分别指在标准规定的测试条件下最低过滤效率为 90%、95%、99.97%。N95不是特定的产品名称。只要符合N95标准, 并且通过NIOSH审查的产品就可以称为“N95型口罩”。
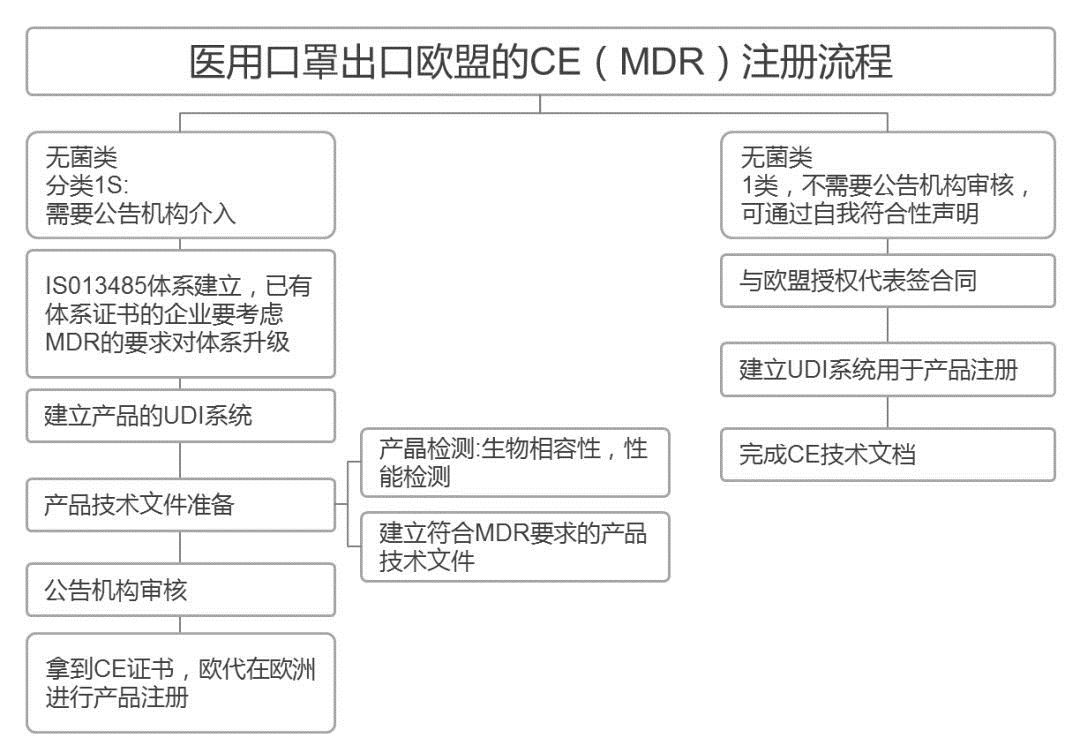
欧盟 必要资料(资质):提单,箱单,发票。 口罩要求: 在欧盟,口罩属于PPE个人防护用品。2019年起,欧盟新法规PPE Regulation(EU)2016/425强制执行, 所有出口欧盟的口罩必须在新法规的要求下获得CE认证证书。CE认证证书的有效期是5年左右, 一般费用是10000~15000元人民币。
欧盟对于口罩欧洲统一,CE认证的标准包括BSEN140、BSEN14387、BSEN143、BSEN149、BSEN136, 其中BSEN149使用多,为可防护微粒的过滤式半口罩,根据测试的粒子穿透率 分为P1(FFP1),P2(FFP2),P3(FFP3)三个等级,FFP1低过滤效果≥80%,FFP2低过滤效果≥94%, FFP3低过滤效果≥97%。 FFP2口罩与上文提到的医用防护口罩、KN95口罩、N95口罩过滤效率十分接近。医疗口罩必须遵循 BSEN14683标准,可以分为三个等级:低标准Type、然后是Type和TypeR。上一个版本是BSEN146832014, 已被新版BSEN146832019所取代。EN 14683:2019年版主要的变化之一是压力差,Type、Type、TypeR 压力差分别由2014年版的29.4、29.4、49.0Pa/cm,上升至40、40、60Pa/cm。 CE认证是欧盟实行的强制性产品安全认证制度,目的是为了保障欧盟国家人民的生命财产安全。
|